

Le diagnostic précis d’un cancer du sein est une étape déterminante pour offrir aux patientes les traitements les plus adaptés et efficaces. Si l’oncologue est souvent mis en avant dans ce processus, ce sont les pathologistes, spécialistes des analyses cellulaire et tissulaire, qui établissent les fondations essentielles du parcours thérapeutique. Leur travail minutieux permet d’identifier précisément les caractéristiques des tumeurs, d’évaluer leur agressivité et de guider les choix thérapeutiques optimaux. Afin de mieux comprendre leur rôle essentiel, nous avons rencontré le Dr. Mohamed Abdou, médecin chef au service d’histopathologie à l’Institut Central des Hôpitaux (ICH) en Valais, ainsi que la Dre. Sophia Taylor, médecin adjointe dans le même service. Ensemble, ils nous expliquent comment leur expertise quotidienne contribue à améliorer la prise en charge des patientes atteintes de cancer du sein.| Adeline Beijns
Pourriez-vous nous expliquer le rôle et l’importance du pathologiste dans le diagnostic du cancer du sein ?
Le rôle du pathologiste dans le diagnostic du cancer du sein est fondamental. Nous analysons les échantillons de tissus prélevés lors de biopsies ou d’interventions chirurgicales pour déterminer avec précision la nature exacte de la tumeur. En plus des analyses histologiques traditionnelles, nous utilisons des technologies avancées telles que la biologie moléculaire pour mieux caractériser les tumeurs. Nous participons également activement à des essais cliniques, ce qui nous permet de contribuer directement à l’amélioration des protocoles diagnostiques et thérapeutiques existants.
Pourriez-vous nous décrire comment s’organise concrètement un laboratoire d’histopathologie, et préciser d’où proviennent les échantillons tumoraux que vous analysez ?
Notre laboratoire d’histopathologie est organisé de manière à garantir efficacité et précision dans le traitement des échantillons. Il regroupe des médecins pathologistes et des techniciens spécialisés qui jouent un rôle clé dans la préparation et la gestion des échantillons. Les prélèvements tumoraux, biopsiques ou chirurgicaux, proviennent de notre hôpital ou d’autres institutions médicales de la région. Dès leur réception, ils sont soigneusement enregistrés, traités selon des protocoles rigoureux, et enfin analysés au microscope.
Quelle approche adoptez-vous spécifiquement pour évaluer une tumeur mammaire, et quelles caractéristiques clés influencent le choix thérapeutique ?
Notre démarche diagnostique commence par l’inspection visuelle et la sélection des zones à analyser (examen macroscopique), suivi de l’analyse microscopique détaillée des tissus. Nous effectuons notamment des tests immunohistochimiques pour déterminer le statut des récepteurs hormonaux, estrogènes et progestérone, et le HER2. L’ensemble de ces informations nous permet de classifier précisément la tumeur et de fournir aux oncologues les éléments nécessaires à la sélection des traitements adaptés, qu’ils soient chirurgicaux, radiothérapeutiques, hormonaux, ciblés, immunothérapeutiques ou chimiothérapeutiques.
Comment formalisez-vous vos observations ? Pouvez-vous nous décrire brièvement le contenu et l’importance du rapport de pathologie ?
Les résultats de nos analyses sont consignés dans un rapport de pathologie très détaillé. Ce document présente clairement toutes les caractéristiques identifiées de la tumeur et offre des indications précises pour la prise en charge thérapeutique. Ce rapport est partagé avec l’équipe clinique afin d’optimiser la prise en charge de la patiente.
Sous quelles différentes formes se présentent les tumeurs mammaires?
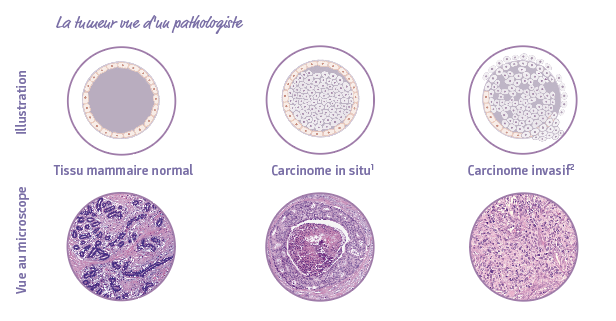
Les cancers mammaires se présentent sous diverses formes, chacune nécessitant des traitements spécifiques. On distingue des carcinomes in situ1 (forme la moins agressive), qui restent confinés dans les canaux du sein, et les carcinomes invasifs2 qui franchissent les limites de ces canaux pour envahir le tissu mammaire adjacent. Parmi ces cancers invasifs, de multiples subdivisions existent selon le type histologique, le grade, la taille, le taux d’expression des récepteurs hormonaux et la surexpression du HER2 impliqué dans la croissance des cellules cancéreuses. Le grade d’un carcinome invasif est déterminé à l’aide d’un score qui repose sur l’évaluation de trois critères morphologiques observés au microscope : l’architecture de la tumeur, les anomalies morphologiques des cellules cancéreuses et le nombre de mitoses. Un score de 1 à 3 points est attribué à chacun de ces critères. La somme de ces points permet d’évaluer la tumeur sur une échelle de 1 à 3, les tumeurs de grade 3 étant les plus agressives. Le récepteur HER2 (Human Epidermal growth factor Receptor 2) est une protéine présente à la surface de certaines cellules humaines normales et impliquée dans la régulation de leur croissance. Si le HER2 est surexprimé (HER2 positif) dans le carcinome invasif, un traitement ciblé peut être administré pour bloquer la croissance tumorale. Si le HER2 est négatif, ces traitements ne sont pas efficaces. Chacun de ces paramètres influence directement le choix du traitement le plus adapté à chaque patiente.
Une fois votre diagnostic posé, quelles sont les étapes suivantes ? Comment partagez-vous ces résultats avec l’oncologue, et en quoi consiste la discussion en tumor board?
Une fois notre diagnostic établi, nous transmettons immédiatement ces résultats au médecin prescripteur. Ces informations sont ensuite discutées au sein d’une réunion multidisciplinaire. Durant ces échanges, les spécialistes examinent les caractéristiques précises de chaque cas, ce qui permet de décider collectivement de la stratégie thérapeutique optimale, garantissant une prise en charge personnalisée et coordonnée.
En complément de votre évaluation initiale, quelles autres technologies utilisez-vous pour mieux comprendre le comportement d’une tumeur et aider l’oncologue à choisir le traitement le plus adapté ?
Afin d’améliorer encore notre capacité à prédire l’évolution de la tumeur, nous recourons à des technologies complémentaires, notamment des tests génomiques et génétiques avancés. Les tests génomiques étudient précisément l’expression de certains gènes à l’intérieur des cellules cancéreuses, permettant d’évaluer plus finement leur comportement biologique et leur potentiel évolutif. Concrètement, ces tests apportent des informations précieuses sur le risque de récidive, la sensibilité probable à certaines thérapies ciblées ou à la chimiothérapie, et contribuent ainsi à individualiser et affiner les décisions thérapeutiques prises par l’oncologue.
Enfin, pourriez-vous nous expliquer ce qu’il advient de l’échantillon tumoral une fois l’analyse histopathologique terminée ?
Après analyse, les échantillons tumoraux sont conservés sous forme de blocs et de lames, soigneusement archivés pour une durée minimale de 20 ans. Cela permet de réexaminer les tissus ultérieurement, que ce soit pour un suivi médical, des analyses complémentaires ou pour investiguer d’éventuelles nouvelles anomalies.
Cet article a été réalisé avec l’aimable soutien d’Exact Sciences International GmbH.
L’indépendance de l’opinion des experts a été entièrement respectée
Exact Sciences est un leader dans le domaine des tests de dépistage et de diagnostic du cancer, offrant la clarté nécessaire pour prendre des mesures décisives et améliorer la prise en charge des patients. Du dépistage précoce du cancer jusqu’à l’orientation vers une prise en charge adaptée et le suivi post-traitement, Exact Sciences aide les personnes concernées à prendre des décisions parmi les plus difficiles avec confiance.

![]()

